Как подготовиться к сдаче анализа
Для получения максимально достоверных данных рекомендуется выполнить ряд подготовительных мероприятий. Они помогут не «смазать» общую картину и точно диагностировать любое отклонение от нормы. Перед забором крови необходимо отказаться от приёма пищи как минимум за 4 часа до этой процедуры. Также накануне рекомендуется исключить тяжелые физические нагрузки, эмоциональные расстройства и стрессы. Принимая какие-либо лекарственные препараты, стоит заранее поговорить с лечащим врачом, который сможет оценить их состав и понять, способен ли их приём повлиять на анализ. Если медикаменты влияют на показатели, то потребуется за несколько дней до сдачи ограничить их употребление. Также нужно отказаться от распития алкогольных напитков и наркотических средств. Для достижения достоверности, перед анализом лучше не курить.
Показатели нормы MCH
Среднее количество гемоглобина в одном эритроците варьируется в зависимости от возраста и пола. Его среднестатистический показатель у взрослого здорового человека составляет от 27 до 31 пикограмм (пг). Наиболее высокие показатели наблюдаются у младенцев, возрастом до 14 дней. Они могут варьироваться от 30 до 37 пг и, по мере взросления, постепенно снижаются и сравниваются с нормой для взрослых.
Нормы у женщин
| Возраст женщины, лет | Норма MCH на один эритроцит (в пг) |
|---|---|
| 16-18 | 26-34 |
| 19-45 | 27-35 |
| 46-60 | 27-34 |
| После 60 | 27-35 |
Нормы у мужчин примерно такие же как и у женщин. Отклонения наблюдаются минимальные.46-6027-34После 6027-35
| Возраст мужчины, лет | Норма MCH на один эритроцит (в пг) |
|---|---|
| 16-18 | 27-32,5 |
| 19-45 | 27-34 |
| 46-60 | 27-35 |
| После 60 | 27-34,5 |
Нормы у детей. Необходимо отметить, что данные показатели нестабильны, они могут менять в течение считанных часов или дней.
| Возраст ребенка, лет | Норма MCH на один эритроцит (в пг) |
|---|---|
| 1-4 месяца | 27-32 |
| 1-3 года | 23-31 |
| 7-15 лет | 26-32 |
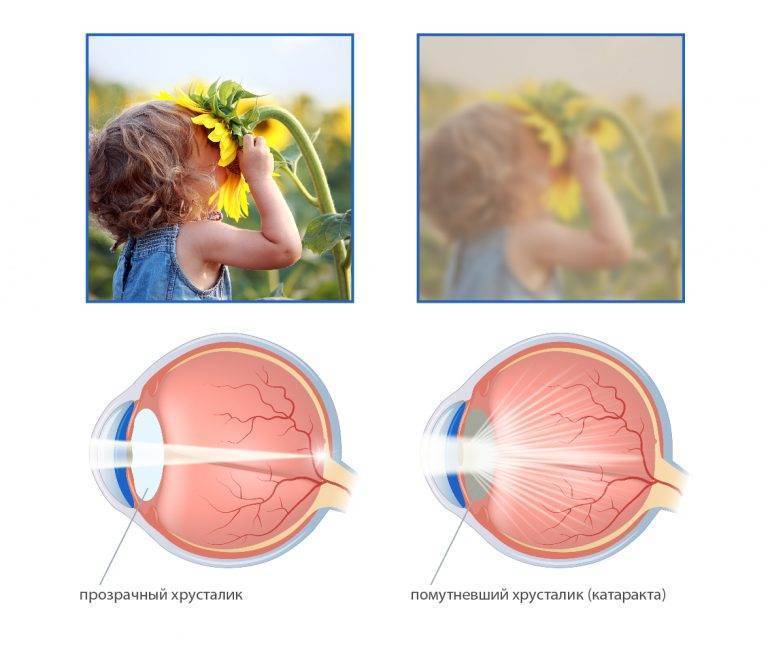
Причины врожденной катаракты
Помутнения в хрусталике новорожденного малыша могут появиться в случаях:
внутриутробного влияния неблагоприятных факторов (внешних и внутренних), действующих на беременную женщину. Ненаследственная врожденная катаракта у детей развивается при воздействии на мать во время вынашивания радиации, интоксикаций, инфекций, резус-конфликта, алкоголя и т.п. Внутриутробная врожденная катаракта – самая распространенная группа помутнений хрусталика, на ее долю приходится 67% всех случаев;
отягощенной наследственности. Чаще патология передается по аутосомно-доминантному типу, но в случае кровного родства родителей появится и при аутосомно-рецессивном варианте наследования. При наследовании, сцепленном с полом, врожденная катаракта у мальчиков проявится в рецессивном типе, у девочек – в доминантном;
при генетически обусловленных нарушениях обмена веществ (галактоземии, врожденной хондродистрофии, синдроме Лоу, псевдогопопаратиреозе и т.п.).
При наследственных болезнях обмена веществ помутнения в хрусталике могут развиться и после рождения малыша.
Врожденные катаракты в половине случаев (от 30 до 70%, по данным разных авторов) сопровождаются другими аномалиями развития глазного яблока – микрофтальмом, аномалиями развития роговицы, колобомами радужки, сосудистой оболочки и пр.
Повышенные и пониженные показатели
Многие люди, когда видят результаты исследований с низким или высоким уровнем гидрокортизона, начинают паниковать и искать у себя опасные для жизни заболевания. Однако далеко не всегда результаты лабораторных исследований указывают именно на них. Даже кортизол у мужчин и женщин в норме будет сильно варьироваться, не говоря про другие факторы. Есть масса обыденных причин, которые могут спровоцировать усиленный синтез
На низкий показатель нужно обратить особое внимание
Понижение: причины и клинические проявления
Если повышенный синтез может быть связан с совершенно нормальными физиологическими изменениями, то низкие показатели говорят о наличии в организме значительной патологии. Клинические признаки отличаются в каждом случае и могут служить возможностью для установки верного диагноза врачом, поэтому при обращении стоит указывать все симптомы изменения гормона кортизола в крови, которые кажутся незначительными.
Виды врожденной катаракты
Детские катарактальные хирурги чаще используют классификацию Хватовой А.В.. Врожденная катаракта глаза бывает:
От характера и степени помутнения напрямую зависят сроки хирургического лечения катаракты.
Общепринятый возраст малыша, при котором риск минимален – 3-6 месяцев. |
При удалении катаракты в более позднем возрасте, особенно при полных формах, велика вероятность низкого функционального результата из-за развития амблиопии.
Детские офтальмохирурги дополнительно выделяют основные клинические формы врожденных катаракт глаза, такие как:
зонулярная. Она отличается наличием оптически прозрачных промежутков в веществе хрусталика. При зонулярной врожденной катаракте острота зрения существенно варьирует от сотых долей до 30-50%;
ядерная. Дисковидное помутнение в ядре, от размера которого зависят зрительные функции;
полярная. Катаракта захватывает участок передней и/или задней капсулы и прилежащего вещества хрусталика в центре. Помутнения менее 2.5 мм в диаметре несущественно снижают остроту зрения;
пленчатая и полурассосавшаяся. Образуются после самопроизвольного лизиса помутнений, характеризуются низким зрением, на уровне 1-4%.
Помимо перечисленных, есть достаточно много других, менее значимых форм врожденной катаракты, практически не снижающих зрение: коралловидная, точечная, порошкообразная и пр.
Анализ на С-реактивный белок
С-реактивный белок (СРБ) – очень чувствительный элемент анализа крови, который быстро реагирует даже на мельчайшее повреждение ткани организма. Присутствие С-реактивного белка в крови является предвестником воспаления, травмы, проникновения в организм бактерий, грибков, паразитов.
СРБ точнее показывает воспалительный процесс в организме, чем СОЭ (скорость оседания эритроцитов). В то же время С-реактивный белок быстро появляется и исчезает – быстрее, чем изменяется СОЭ.
За способность С-реактивного белка в крови появляться в самый пик заболевания его еще называют «белком острой фазы».
При переходе болезни в хроническую фазу С-реактивный белок снижается в крови, а при обострении процесса повышается вновь.
С-реактивный белок норма
С-реактивный белок производится клетками печени и в сыворотке крови содержится в минимальном количестве. Содержание СРБ в сыворотке крови не зависит от гормонов, беременности, пола, возраста.
Норма С-реактивного белка у взрослых и детей одинаковая – меньше 5 мг/ л (или 0,5 мг/ дл).
Анализ крови на С-реактивный белок берется из вены утром, натощак.
1
Анализ крови на уровень мочевой кислоты
2
анализ крови на антинуклеарные антитела
3
Исследование крови на ревматоидный фактор
Причины повышения С-реактивного белка
С-реактивный белок может быть повышен при наличии следующих заболеваний:
- ревматизм;
- острые бактериальные, грибковые, паразитарные и вирусные инфекции;
- желудочно-кишечные заболевания;
- очаговые инфекции (например, хронический тонзиллит);
- сепсис;
- ожоги;
- послеоперационные осложнения;
- инфаркт миокарда;
- бронхиальная астма с воспалением органов дыхания;
- осложненный острый панкреатит;
- менингит;
- туберкулез;
- опухоли с метастазами;
- некоторые аутоиммунные заболевания (ревматоидный артрит, системный васкулит и др.).
При малейшем воспалении в первые же 6-8 часов концентрация С-реактивного белка в крови повышается в десятки раз. Имеется прямая зависимость между тяжестью заболевания и изменением уровня СРБ. Т.е. чем выше концентрация С-реактивного белка, тем сильнее развивается воспалительный процесс.
Поэтому изменение концентрации С-реактивного белка используется для мониторинга и контроля эффективности лечения бактериальных и вирусных инфекций.
Разные причины приводят к разному повышению уровня С-реактивного белка:
- Наличие бактериальных инфекций хронического характера и некоторых системных ревматических заболеваний повышает С-реактивный белок до 10-30 мг/л. При вирусной инфекции (если нет травмы) уровень СРБ повышается незначительно. Поэтому высокие его значения указывают на наличие бактериальной инфекции.
- При подозрении на сепсис новорожденных уровень СРБ 12 мг/л и более говорит о необходимости срочной противомикробной терапии.
- При острых бактериальных инфекциях, обострении некоторых хронических заболеваний, остром инфаркте миокарда и после хирургических операциях самый высокий уровень СРБ – от 40 до 100 мг/л. При правильном лечении концентрация С-реактивного белка снижается уже в ближайшие дни, а если этого не произошло, необходимо обсудить другое антибактериальное лечение. Если за 4-6 дней лечения значение СРБ не уменьшилось, а осталось прежним и даже увеличилось, это указывает на появление осложнений (пневмония, тромбофлебит, раневой абсцесс и др.). После операции СРБ будет тем выше, чем тяжелее была операция.
- При инфаркте миокарда белок повышается через 18-36 часов после начала заболевания, через 18-20 дней снижается и к 30-40 дню приходит к норме. При стенокардии он остается в норме.
- При различных опухолях повышение уровня С-реактивного белка может служить тестом для оценки прогрессирования опухолей и рецидива заболевания.
- Тяжелые общие инфекции, ожоги, сепсис повышают С-реактивный белок до огромнейших значений: до 300 мг/л и более.
- При правильном лечении уровень С-реактивного белка снижается уже на 6-10 день.
Подготовка к ревматологическим анализам
Чтобы анализы показывали объективную информацию, необходимо придерживаться некоторых правил. Сдавать кровь нужно в утренние часы, натощак. Между взятием анализов и приемом пищи должно пройти приблизительно 12 часов. Если мучает жажда, выпейте немного воды, но не сок, чай или кофе. Необходимо исключить интенсивные физические упражнения, стрессы. Нельзя курить и употреблять спиртное.
Клиническая картина
Первые симптомы Г. (рвота, падение веса, желтуха) могут появиться вскоре после рождения, как только ребенок начинает получать молоко, позднее возникают прогрессирующая гепатомегалия, асцит, диспептические расстройства, в дальнейшем появляется катаракта, арефлексия, задержка психомоторного развития.
При тяжелой форме Г. смерть наступает через несколько месяцев. При легкой форме заболевания указанные симптомы менее выражены, но, как правило, отмечаются рвота, задержка роста и развития, гепатомегалия, катаракта.
Асимптоматическая форма случайно обнаруживается в семьях, в к-рых есть или были больные Г. Дети из этих семей развиваются нормально; характерно, что они не любят молока и часто отказываются от груди.
Какие анализы сдают на беременность
Основной анализ называется кратко “ХГЧ” и основывается на выявлении в крови концентрации специфического маркера зачатия. Это особый гормон у беременной женщины. Он вырабатывается клетками хориона (оболочки зародыша), обеспечивая существование желтого тела и развитие эмбриона.
Определение ХГЧ в сыворотке крови – основа анализа на беременность: его концентрация в крови растет в геометрической прогрессии и в первый день задержки менструального цикла достигает 25 мМЕ/мл. На основании этого исследования гинеколог определяет присутствие в организме хориальной ткани, а значит – зачатие ребенка у женщины. Сдача крови на беременность делает возможным уже на 9-12 день после полового акта установить факт оплодотворения. Пик концентрации ХГЧ – между 8-10 неделями беременности, затем начинает снижаться. При многоплодной беременности в анализах уровень ХГЧ будет выше.
Сроки беременности по крови – норма ХГЧ по неделям
| Недели беременности * | Норма, мМЕ/мл |
|---|---|
| Беременность 2-3 недели | 10,0-50,0 |
| 4 недели | 40,0-6.000 |
| 5 недели | 1.000-20.700 |
| 6 недель | 2.200-74.200 |
| 7 недель | 6.000-130.000 |
| 8 недель | 12.900-190.000 |
| 9 недель | 18.500-205.000 |
| 10 недель | 18.000-290.000 |
| 11 недель | 16.500-180.000 |
| 12 недель | 14.500-125.000 |
| 13 недель | 12.500-95.000 |
| 14 недель | 10.500-80.000 |
| 15 недель | 9.000-70.000 |
| 16 недель | 7.000-64.000 |
| 17 недель | 5.500-56.000 |
| 18 недель | 4.500-50.000 |
| 19 недель | 3.300-40.000 |
| 20 недель | 2.500-32.000 |
| 21-26 недели | 1.800-25.000 |
| 26-43 недели | 1.800-59.000 |
| Мужчины | ХГЧ < 5,0 |
| Небеременные женщины | ХГЧ < 5,0 |
* Указаны акушерские недели. Акушерский срок начинается с первого дня последней менструации.
Когда еще нужно сдать кровь при беременности
Регулярный мониторинг показателей ХГЧ во время вынашивания плода является методом контроля за нормальным его развитием, т.н. “пренатальный скрининг”. Сдают анаизы на ХГЧ в установленные сроки для выявления возможных патологий. Пониженный уровень гормона в крови может свидетельствовать о неразвивающейся или внематочной беременности, угрозе выкидыша.
Однако, чтобы пренатальная диагностика была более достоверной, сдают не один ХГЧ. Вместе с ним проверяются следующие маркеры: АФП, Е3 (альфа-фетопротеин, свободный эстриол), делается УЗИ скрининг с последующей интерпретацией результатов согласно установленных регламентов.
Правила сдачи анализа на беременность
- Сроки, когда анализ покажет беременность – это 1-2 день задержки менструации и более;
- Какая достоверность – около 99%, меньще – если тест проводится до задержки;
- Сдают этот анализ натощак (не менее 3-4 и не более 14 часов голодания). Без ограничений можно пить воду без газа.
- Сроки готовности теста – 6-8 часов с момента сдачи.
- Как можно получить ответ быстрее? Кровь у нас в клинике сдаётся с 10.00 – 20.00. по будням, и до 17.00 в субботу и воскресенье. Если Вы хотите ускорить получение результата анализа и узнать, есть беременность или нет в тот же день, постарайтесь быть у нас с 10.00 до 12.00!
Цена анализа крови на беременность – 550 рублей;Взятие крови из вены – 450 рублей.
home
Где сдать кровь на беременность в Москве
Если есть хоть сомнения в наличии или отсутствии беременности, сдайте анализ на беременность с первого дня задержки месячных. При положительном результате сделайте УЗИ для уточнения расположения плодного яйца и посетите гинеколога. В случае, если кровь покажет отрицательный результат, а задержка есть и нет месячных, то посетите гинеколога-эндокринолога для уточнения причин нарушения цикла. Приглашаем в наш медицинский центр!
Взятие материала в течении всего рабочего дня, с 10-00. Срок готовности: если сдать анализы крови с 10 до 12-00 – то результат можно получить в тот же день вечером; если сдаете после 12-00 – то на следующий день. Узнать ответ можно по телефону или получить на электронную почту.
Положительный анализ на беременность?Что делать дальше:Ведение
беременности Прерывание
беременности
Что такое лактазная недостаточность?
Расщепление молекулы лактозы на составные части происходит в тонкой кишке. Для этого процесса нужен особый фермент – лактаза.
Лактазная недостаточность – это нарушение, развивающееся в результате снижения количества или активности фермента лактазы.
Выделяют два вида лактазной недостаточности – первичная (врожденная и транзиторная/временная) и вторичная (приобретенная).
Первичная (врожденная) лактазная недостаточность.
Это наследственная, генетическая аномалия. Эта особенность выявляется в среднем у 5 – 6 процентов населения земного шара, в каких-то регионах меньше, в каких-то больше. Она характеризуется дефицитом фермента лактазы при нормальной, неповрежденной слизистой кишечника. Причиной этого является врожденная мутация генов. Дети с такой особенностью не будут переносить лактозу в течение всей своей жизни.
Первичная (транзиторная) лактазная недостаточность.
Чаще всего родители грудничков сталкиваются именно с ней. Как правило, она встречается у недоношенных или незрелых к моменту рождения детей. Дело в том, что в течение внутриутробного развития способность кишечника ребенка вырабатывать фермент лактазу возрастает постепенно, достигая максимума к моменту рождения. А это значит, что у деток, родившихся преждевременно, лактазы вырабатывается меньше, чем у детей, родившихся в срок. Однако недостаток лактазы будет не постоянным, а временным (транзиторным).
По мере роста и развития ребенка его желудочно-кишечный тракт будет созревать, соответственно, и выработка, и активность фермента будут повышаться. Обычно к 3-4 месяцам количество и активность фермента достигает нормы, и симптомы лактазной недостаточности постепенно проходят.
Факторами, негативно влияющими на выработку лактазы у малыша, кроме недоношенности, являются также: хроническая фетоплацентарная недостаточность во время беременности, угроза ее прерывания, другие осложнения беременности, а также отдельное от мамы пребывание в роддоме, раннее отлучение от груди.
Вторичная (приобретенная) лактазная недостаточность.
Развивается при каких-либо заболеваниях кишечника как инфекционной, так и неинфекционной природы. Повреждение клеток кишечника (энтероцитов) ведет к снижению синтеза лактазы. В результате развивается лактазная недостаточность. Обычно это явление временное, при стихании патологического процесса синтез фермента восстанавливается.
У грудничков и детей младшего возраста вторичная лактазная недостаточность может случиться на фоне кишечных инфекций как вирусного, так и бактериального происхождения. В этих случаях имеет место как прямое повреждение клеток кишечника инфекционным агентом, так и развитие последующего нарушения состава микробиоты в нем (т.н. дисбактериоза).
Лямблиоз также является частой инфекцией среди детей, особенно в возрасте от 1 до 4 лет. При лямблиозе нарушается процесс расщеплении лактозы.
Наличие выраженного нарушения микрофлоры кишечника само по себе, безотносительно кишечной инфекции, может провоцировать развитие лактазной недостаточности.
Нарушение микрофлоры отмечается, например, в результате приема антибиотиков. Также нарушение микробиоты кишечника взаимосвязано с аллергическими процессами.
Истинная целиакия (глютеновая энтеропатия) – редкое заболевание, при котором происходит повреждение ворсинок тонкого кишечника продуктами, содержащими глютен. При целиакии в слизистой тонкого кишечника снижается количество всех ферментов, в том числе и лактазы.
Диагностика галактоземии
В РФ неонатальный скрининг на ГЕ осуществляют доношенным новорожденным на 4-е сутки жизни, а недоношенным на 7-е сутки жизни. Определяют уровень тотальной галактозы, который в норме < 7,2 мг/дл. Если ее уровень превышает референсное значение, проводят ДНК-диагностику для детекции мутаций в гене GALT. Определяют активность фермента ГАЛТ: снижение его активности в пятнах высушенной крови < 2,5 Е/гHb, в цельной крови < 1,3 Е/гHb является диагностически значимым. Если активность ГАЛТ превышает референсное значение на 50%, а симптомы ГЕ отсутствуют, либо незначительны, специальное лечение не проводится. Успешно проводится и пренатальная диагностика.
Как проводится исследование
Для получения данных о МСН в анализе крови осуществляется забор крови из вены. В редких случаях возможно использование капилляров пальца (сейчас практически не используется, так как отличается меньшей точностью и информативностью). Данная процедура выполняется медицинской сестрой или работником лаборатории, имеющим соответствующее образование и лицензию на осуществление этой деятельности. Её длительность составляет не более 5 минут и сопровождается незначительной болезненностью и дискомфортом в месте прокола. Однако неприятные ощущения быстро исчезают, а на месте прокола может остаться небольшой синяк. Лицам, испытывающим страх от вида крови, настоятельно рекомендуется отвернуться и не смотреть на руку до окончания процедуры. Но для предотвращения потери сознания и быстрого введения в чувство в кабинете всегда присутствует ватный диск и нашатырь. Забор крови проводится в несколько последовательных стадий:
- Наложение резинового или тканевого жгута с фиксаторами на предплечье пациента, который должен немного поработать кулаков (несколько раз сжать и разжать руку для лучшего наполнения сосудов).
- Лаборант или медсестра выбирает наиболее подходящую вену и обрабатывает кожу спиртовым тампоном.
- Введение иглы в вену, по которой кровь поступает в шприц или специальную пробирку. Зачастую, набирается не более 5 мл.
- Извлечение иглы и накладывание на место прокола ватки, смоченной в спирте.
Для предотвращения появления кровоподтёков или формирования синяков, пациента просят на несколько минут прижать предплечье к плечу. На этом процедура заканчивается и медицинский работник подписывает пробирку, после чего полученный материал размещается в анализаторе. Его использование даёт возможность в автоматическом режиме подсчитать все виды кровяных клеток, включая эритроциты. Полученные данные отправляются лечащему врачу, после чего начинается расшифровка анализа крови МСН.
Описание
Галактоземия относится к ряду врожденных наследственных патологий. Встречается это заболевание в медицинской практике достаточно редко.
Связывают развитие патологии с недостаточной активностью необходимых для нормального процесса обмена веществ ферментов, «перерабатывающих» галактозы.
Впервые описали клинику галактоземии в 1908 г. (хотя некоторые относят к данному факту только 1917 г.). К сожалению, но подопытным ребенком стал тот, который страдал истощением, увеличением селезенки и печени. Утверждается, что вся эта симптоматика исчезла после того, как малышу отменили молочное питание.
Общее описание
 Галактоземия (ГЕ) — это наследственно обусловленное нарушение углеводного обмена, при котором происходит накопление галактозы и ее метаболитов: галактозо-1-фосфата и галактитола в организме, а их токсическое действие приводит к многочисленным нарушениям его функций. Неоценимое значение галактозы для развития ребенка заключается в том, что она является компонентом молока. ГЕ встречается примерно у одного новорожденного из 16 тысяч.
Галактоземия (ГЕ) — это наследственно обусловленное нарушение углеводного обмена, при котором происходит накопление галактозы и ее метаболитов: галактозо-1-фосфата и галактитола в организме, а их токсическое действие приводит к многочисленным нарушениям его функций. Неоценимое значение галактозы для развития ребенка заключается в том, что она является компонентом молока. ГЕ встречается примерно у одного новорожденного из 16 тысяч.
ГЕ передается потомству по аутосомно-рецессивному типу. Семья, уже воспитывающая больного ребенка, имеет риск 1:4 появления нездорового младенца при следующей беременности. Самая распространенная, т.н. классическая форма ГЕ, обусловлена мутацией гена GALT, локализованного в 9p13.3 из-за чего происходит недостаток фермента галактозо-1-фосфатуридилтраснферазы (ГАЛТ), отвечающего за метаболизм галактозы. Галактоза является строительным материалом для мембран клеток, волокон нервной системы, являясь одновременно источником энергии для клетки. Токсические же продукты ее метаболизма, тормозят действие ферментов фосфоглюкомутазы и глюкозо-6-фосфатдегидрогеназы, еще одних участников углеводного обмена, что влечет за собой гипогликемию, а также блокируют антибактериальную активность лейкоцитов, что инициирует сепсис новорожденных. При несвоевременной медицинской помощи, примерно ¾ больных погибают уже в младенческом возрасте.
Что делать, если ЛДГ не в норме?
Для того чтобы нормализовать уровень фермента, нужно в первую очередь выяснить почему возникли отклонения. Только установив причины пониженного ЛДГ в крови и устранив основное заболевание, которое является катализатором, будет возможность вернуть значения к нормальному диапазону. Для определения причины необходимо пройти детальное обследование, так как каждая патология имеет свои нюансы лечения. При анемии проводят коррекцию питания и назначают препараты для восстановления баланса железа, при онкологических заболеваниях назначают масштабный скрининг больного, в случае острых форм патологий определяют стационарное лечение.
Патология тимуса
Основные виды патологии тимуса:
- Аплазия – отсутствие или недоразвитие вилочковой железы
- Гипо- и дисплазия – недоразвитие тимуса
- Акцидентальная инволюция – уменьшение вилочковой железы, под влиянием гормонального дисбаланса, стресса, инфекции
- Атрофия – уменьшение, замещение железистой ткани соединительной, прекращение функционирования
- Тимомегалия – увеличение массы и объема паренхимы вилочковой железы выше возрастной нормы при сохранении ее нормального строения
- Гиперплазия – увеличение железистой ткани, с нарушением выработки иммунных клеток и функционирования тимуса.
- Тимома – опухоль вилочковой железы.
- Киста тимуса – жидкостное образование вилочковой железы.
- Патология тимуса (вилочковой железы) может вызывать: развитие ряда иммунодефицитных синдромов, аутоиммунных заболеваний и некоторых эндокринных нарушений.
Степени тяжести
1. Легкая, при которой симптомы галактоземии видны лишь спустя 7–10 дней. Признаки болезни незначительны, токсическое воздействие моносахарида проявляется в нарушении функционирования печени (хронические патологии). Одним из признаков легкой формы галактоземии является непереносимость ребенком молока, отказ от груди.
При малосимптомном течении галактоземия поражает ЦНС, глаза, может беспокоить диспепсический синдром. Также известны случаи бессимптомного течения. Диагностика этой формы галактоземии состоит в проведении ферментного анализа.
2. Средняя степень наследственной патологии галактоземии проявляется у детей следующим образом:
- Нарушение пищеварения, потеря веса, рвоты;
- Печень в течение всего нескольких дней увеличивается в размерах;
- Желтый цвет кожи разной степени выраженности;
- Развитие анемии;
- Слизистая глаз меняется, появляется желтушность и помутнение хрусталика (свидетельствует о появлении катаракты);
- Ребенок довольно апатичен либо же, наоборот, перевозбужден (проявления со стороны ЦНС);
- Малыш «не успевает» догнать здоровых сверстников, со временем отставая в развитии двигательного аппарата, органов чувств.
3. Если степень болезни тяжелая, то симптомы галактоземии развиваются почти молниеносно в самые первые дни после рождения. Кормление молоком с лактозой вызывает:
- Рвоту, обычно такую обильную, что развивается стремительное истощение;
- Жидкие испражнения;
- Колики и отхождение газов;
- Интоксикация, отказ от груди (либо бутылочки);
- Свойственные новорожденным рефлексы угасают;
- Желтушность и увеличение размеров печение, поражение почек;
- В возрасте 1–2 месяца диагностируется двусторонняя катаракта;
- Симптомы галактоземии в возрасте 2–3 месяцев – это цирроз, жидкость внутри брюшной ямы, увеличение селезенки (спленомегалия);
- Кровоизлияние (на слизистых, коже – из-за нарушения свертываемости);
- Со временем развивается нарушение интеллекта;
Диагностика
Неонатальный скрининг. Первичное обследование, проводимое с целью выявления наследственной галактоземии у родившихся детей, проводится после рождения. Если ребенок доношенный, то скрининг делается на 3–5 день, а если не доношен, то в конце первой недели жизни.
Биохимия крови, исследование мочи для выявления количества моносахарида. В моче определяется галактозурия, протеинурия (белок), мелитурия (выделение сахаров), аминоацидурия (выделение аминокислот).
Чтобы узнать степень повреждения внутренних органов, проводится мониторинг параметров крови, мочи.
Устанавливается факт генетической болезни у родственников.
Дополнительно в целях диагностики галактоземии проводятся тесты с глюкозой, галактозой.
УЗИ живота.
ЭЭГ – исследование мозга, его функционирования, происходящих в нем сдвигов, локализации патологий.
Консультирование узких врачей (детский офтальмолог, детский невролог).
Диагностика галактоземии также включает в себя ряд методов, служащих для определения других заболеваний, схожих по симптоматике. Проводятся обследования на наличие сахарного диабета, патологий печени, гемолитической болезни, гликозурии, гликогенозов.
Симптомы
Наиболее важные проявления патологии – это непереносимость любого молока, в составе которого имеется лактоза, а также развитие желтухи, катаракты (сложная болезнь глаз), гепатомегалии, цирроза, истощения ввиду нарушения пищеварения.
Симптомы галоктоземии у новорожденных развиваются из-за значительного повышения концентрации токсичных веществ в крови и появления реакции торможения ферментов на активность токсинов. Ферменты, участвующие в метаболизме углеводов, не могут снизить плотность галактозы (а также ее обменных продуктов), поэтому развивается гипогликемический синдром, оказывающий негативное влияние на ряд внутренних органов.
Распространенные признаки галактоземии. Виды патологии
Классический: обусловлен недостатком галактозо-1-фосфат уридилтрансферазы (это фермент, который участвует в преобразовании галактозы в глюкозу). При недостаточном количестве этого фермента происходит повышение галактозы в крови и уменьшение глюкозы. Печень неполноценно участвует в обмене D-галактозы (составной части молока). Симптомы галактоземии при классическом типе – это большая масса тела новорожденного ребенка. Дополнительно в ближайшее время после родов, после того, как малыш выпьет молоко, у него возникает жидкий стул и/или сильная рвота. Стремительно развивается гипотрофия (дефицит массы тела, истощение), появляется пожелтение склер глаз, кожи. Печень увеличивается, развиваются признаки катаракты (она вызвана образованием галактита в глазном хрусталике по причине расстройства электролитного баланса и повышения галактозы). Часто развивается гемолитическая форма анемии (распад эритроцитов).
Недостаточность галактокиназы проявляется только одним признаком – развитием катаракты. Чтобы понять, что у новорожденного ребенка развивается именно галактоземия, исследуются биологические жидкости. Анализ крови покажет увеличение галактозы и галактитола. Моча насыщается восстанавливающими веществами. Симптомы катаракты развиваются очень быстро, и галактоземия прогрессирует при отсутствии лечения. При своевременной терапии патологические процессы в глазах обратимы.
Недостаточность эпимеразы мало изучена. Патология этого типа почти не имеет физических проявлений, отмечается биохимическими сдвигами, выявляемыми случайно (обнаруживается повышение моносахарида). Данный тип болезни не требует экстренной терапии.
Галактоземия у новорожденных выдает симптоматику в первые 3–10 дней после рождения. В организм ребенка поступает молоко, а вместе с ним вещества, которые не могут перевариться и усвоиться. Постепенно токсины накапливаются. Метаболизм фермента протекает в печени, после чего он поступает в кровяное русло.